有机氟化物的物理性质
有机氟化物的物理性质由两个主要因素控制:①高的电负性和较小的原子半径,氟原子的2s和2p轨道与碳原子的相应轨道特别匹配;②上述原因也导致氟原子特别低的可极化性。
在所有的元素中,氟具有最高的电负性(3.98),使得C-F键高度极化,它的偶极矩大约在1.4D,这还取决于不同的化学环境(参见表1.3)。这与我们观察到的,全氟烷烃(PFCs)却是属于极性最低的溶剂[例如C6F14 (3)的介电常数ε=1.69,而己烷C6H14 (1)为1.89,见表1.4],似乎有矛盾。对这样一个表面看来存在明显矛盾的解释是因为全氟烷烃分子中所有局部的偶极矩相互抵消,导致整个分子没有极性。半氟化的化合物,例如2(C3H7-C3F7),其分子中的局部偶极矩无法相互抵消,总偶极矩可以通过自身的物理化学性质反映出来,尤其是它们的汽化热(△Hv)和介电常数(ε)。
表1.3碳卤键及碳碳键特征之比较(电负性数据引自参考文献;范德华半径数据引自参考文献;原子极化率数据引自参考文献
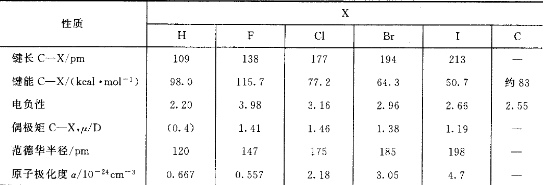
表1.4己烷(1)、半氟己烷(2)和全氟己烷(3)物理化学性质之比较

氟原子仅比氢原子稍大(范德华半径比氢原子大23%)而且具有较低的可极化度,因此全氟烷烃的分子结构及分子动力学也受到影响。直链烷烃是线性锯齿形构型(图1.2)。相反,由于碳链1,3-位(即间位)碳原子上连接的电荷上“极硬的”氟原子之间的立体排斥作用,全氟烷烃PFC。具有螺旋形结构。而直链烷烃的碳链具有一定柔性,全氟烷烃的碳链却是刚性的棒状分子结构。这种刚性可归因于1,3-位上两个二氟亚甲基基团(-CF2-)的排斥张力。

图1.2正辛烷的锯齿形构型(a)和全氟辛烷的螺旋形结构(b)对比,基于PM3理论水平的分子模型
全氟烷烃的低可极化性质引起的另一个结果是分子间很低的散射作用。全氟烷烃的一个突出特征是与相似相对分子质量的烷烃相比其沸点要低得多。例如正己烷和CF4相对分子质量相近(Mr分别为86g·moL-1和88g·moL-1),但CF4的沸点(-128℃)却比正己烷n-C6H14(69℃)低近200℃。如果将它们的同系物做一比较(图1.3),尽管PFCs的相对分子质量比相应碳氢化合物高出近四倍,但它们的沸点几乎相同。
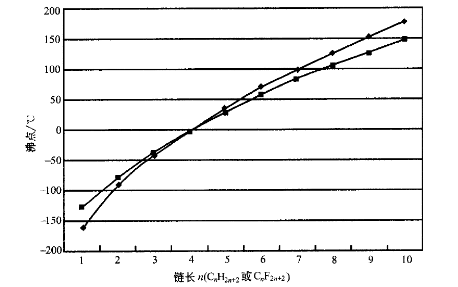
链长n(CnH2n+2或CuF2n+2)
图1.3直链烷烃同系物(初和相应全氟烷烃同系物(·)的沸点比较
与一般碳氢烷烃相反,全氟烷烃上的支链对它的沸点影响很小(图1.4)。
全氟胺、醚和酮通常比它的碳氢类似物的沸点要低得多。
还有一个颇有趣的特征是全氟烷烃的沸点仅比其相对分子质量相近的惰性气体高25~30℃(Kr, Mr 83.8g·moL-1,b.p.-153.4℃;Xe, Mr 131.3g·mol-l,b.p-108.4℃; Rn, Mr 222g·mol-1,b.p.-62.1℃)。另一方面,全氟烷烃的化学活性也与惰性气体相近。
由于全氟烷烃的低可极化性造成与其他碳氢溶剂的互溶性很差,因此就产生了所谓液相的第三相,即除有机相和水相以外的“氟相”。对此,目前已经进行了广泛的研究并称之为氟相化学。
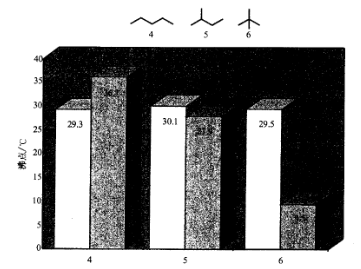
图1.4全氟戊烷(白色柱)和戊烷(灰色柱)的直链和支链的异构体沸点数据
由于全氟烷烃微弱的分子间相互作用而呈现出另一非常突出的特点,是其极低的表面张力(γ)。在所有有机液体中全氟烷烃具有最低的表面张力(示例见表1.4),因而它能够润湿几乎任何物质表面。
固体全氟烷烃的表面也具有极低的表面能(γc)。PTFE(Teflon,特氟龙,聚四氟乙烯)的表面能为18.5dyn·cm-1,使其具有不粘性和低摩擦性,能应用于煎锅等其他领域。这一性质与氟含量直接相关,比较一下几个聚合物的表面能就可了解:聚偏氟乙烯(25dyn·cm-1),聚氟乙烯(28dyn·cm-1)、聚乙烯(31dyn·cm-l)。若聚四氟乙烯中的一个氟原子被易极化的氯原子所取代,由此生成的聚三氟氯乙烯的表面能即升高至31 dyn·cm-1,与聚乙烯相同。
低表面能的形成一可以确定是由于氟原子紧密覆盖的表面所致。因此,所有能观察到的具有最低表面能的材料是氟化石墨(C2F)n、和(CF)n ,它的表面能仅约6dyn·cm-1。单分子层的长链全氟羧酸CF3(CF2)nCO2H(n≥6)的表面能介乎6~9dyn·cm-1。在含有相对较短全氟链[至少CF3(CF2)6]的羧酸系列中也观察到同样的影响。
当一个全氟碳链上联接一个亲水基团时就得到一个含氟表面活性剂(如n-CnF2n+1 COOLi, n≥6),它一可以将水的表面张力从72dyn·cm-1降低到15~20dyn·cm-1。而类似的碳氢表面活性剂仅能降低到25~35dyn·cm-1。
一种所谓的两嵌段两性分子F(CF2)m(CH2)nH,是一种最不同寻常的表面活性剂,在它们的分子中,兼有碳氢和全氟烷基基团。其在有机相和“氟相”(如液态全氟烷烃PFC)的界面间显示出典型的表面活性剂行为,例如胶束的形成。
全氟烷烃分子间的相互作用是非常弱的,但由于存在局部的不能抵消的碳-氟偶极相互作用,一些部分氟化的烷烃(即氢氟烷烃HFCs)存在着相当强的静电相互作用。氟原子和氢原子键合在同一碳原子上时可以观察到最明显的此类作用存在。在此环境下极化的C-H键可作为氢键的供体,而氟原子则是受体。这种影响最简单的例子是二氟甲烷,可以比较一下甲烷和各种不同氟代甲烷的沸点(图1.5),非极性的甲烷和四氟甲烷的沸点最低;稍有极性的CH3F和CF3H沸点稍高。二氟甲烷的沸点最高,它具有最强的分子偶极矩,能够(至少在理论上)形成像水一样的三维氢键网络,其中C-H作为氢键的供体,而C-F键作为氢键的受体(图1.6)。
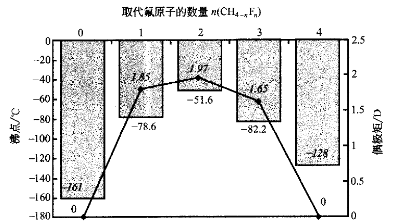
图1.5甲烷和各个不同的氟代甲烷(CH4-nFn)的沸点(℃,灰色棒)和偶极矩(D),(◆,以斜体数字给出)
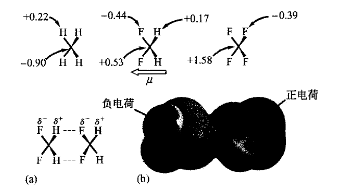
图1.6 (a)部分电荷q(e)在CH4, CH2F2, CF4分子中的分配比较(MP2/6-31+G**理论水平); (b)双重氢键桥联的二氟甲烷二聚体的计算结构(AM1)。基于电子等密度面的静电势图
在苯和全氟苯之间观察到是一种不同类型的强静电作用(有关详细内容请参阅文献,苯(熔点5.5℃,沸点80℃)、全氟苯(熔点3.9℃,沸点80.5℃),二者的相转变温度相近。相比之下,当二者以等摩尔混合后,可以形成熔点为23.7℃的1:1共晶体,比两个单一化合物熔点均高出约19℃。苯和全氟苯的晶体都是边一面鱼骨状结构,而苯-氟苯共晶体则是交替倾斜平行排列的,堆积的层与层之间距离约为3.4Ao,中心一中心距离约为3.7Ao(图1.7)。而相邻的堆积之间又因有Caryl-H…F之间的相互作用而更稳定。

图1.7苯和全氟苯1:1的配合物的X衍射晶体结构图,在30K最低温度下测得
其他芳香化合物一全氟芳香化合物的配合物也可以观察到类似的结构,这表明了此类相互作用在这类结构中是普遍存在的现象。基于结构、光谱数据和量子化学计算(图1.8)的证据,表明,上述所观察到的芳香化合物与全氟芳香化合物的相互作用主要是强烈的四极静电吸引的结果。
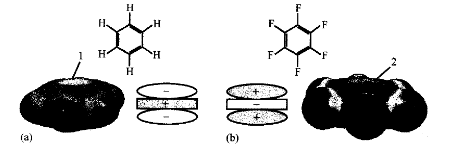
图1.8苯(a)(-29.0×10-40C·m-2)和全氟苯(b)(+31.7×10-40 C·m-2)的互补四极矩图解。图中颜色表示分子表面的静电势能图(B3LYP/6-31G*理论水平)。苯(最左边)最大的负电荷电子密度(1)分别在π体系平面的上下方;相反在全氟苯(最右边)平面的上下方却是分布着部分正电荷(2)
普通的相互作用如“芳环堆积力”,一种距离的负6次方(r-6)相关的色散相互作用,在此种现象中似乎也起着重要的补充作用。另一方面,根据光谱数据分析,排除了由富电子的苯与缺电子的氟苯形成一个电荷转移络合物的可能性。苯和全氟苯的四极矩分别是-29.0×10-40 C·m-2和+31.7×10-40 C·M-2,数量级相同但符号相反而形成互补对,其相互作用大小与其距离的负5次方(γ-5)相关。四极相互作用的方向性是芳环堆积并优先形成类似三明治结构互补排列的固体状态的主要驱动力。根据从头计算法和密度函数理论(DFT)计算可以确定其在平行排列行之间相互作用的能量在-3.7~5.6kca·mol-1(假定平面分子间距离为3.6Ao),这与从杂二聚体的晶体结构中测试得到的值有少许偏差。混杂二聚体的相互作用能要比单纯苯或全氟苯二聚体高1.5~3倍。另一个来自于计算的有趣结果是色散相互作用对杂二聚体的总结合能的贡献甚至要高于静电作用力。
由于C-F键的极化性质所产生的静电相互作用对于具有生理活性的含氟化合物的功效和对含氟液晶的中间相行为起着重要作用。而全氟分子亚结构的低可极化性的特性也已得到许多商业上的应用,如氟氯烷烃制冷剂,化学灭火剂,润滑剂,具有不粘性和低摩擦性能的含氟聚合物和含氟表面活性剂。
【关键词】全氟己烷 正辛烷 聚四氟乙烯 二氟甲烷

随着电子产品防水需求的不断提高,从原先的 IP54到现在的IP67IP68等级!市场上出现了防水透气膜和防水透音膜,目前这两种不同的材料应用被搞混了,今天便与大家一起讨论防水透气
最近各地降雨量激增,所以手机就难免会沾点水,作为生活中不可或缺的电子产品,防水已经成为一个十分重要重要功能,而且个人对目前的IP68手机市场是相当不满意的。为什么?太贵
自然界中荷叶具有出淤泥而不染的典型不沾水特性(学术上称为Cassie-Baxter状态),具有自清洁、抗结冰、减阻、抗腐蚀等广泛应用价值,而玫瑰花瓣则具有水滴高粘附特性(称为Wenze

派瑞林各种粉材真空镀膜技术加工 纳米涂层防水处理
派瑞林各种粉材真空镀膜技术加工 纳米涂层防水处理

高阻隔强绝缘防汗液涂层蓝牙耳机3C电子产品IPX7纳米材料
高阻隔强绝缘防汗液涂层蓝牙耳机3C电子产品IPX7纳米材料

耐磨超疏水纳米材料 绝缘子架空导线电缆桥梁防覆冰涂层
耐磨超疏水纳米材料 绝缘子架空导线电缆桥梁防覆冰涂层

真空等离子气相沉积技术纳米防水镀膜加工 产能5万片天
真空等离子气相沉积技术纳米防水镀膜加工 产能5万片天
亲水疏油自洁净纳米涂层 易去污 无机防紫外高硬度材料
亲水疏油自洁净纳米涂层 易去污 无机防紫外高硬度材料

台湾超亲水防雾塑料专用 附着力好 透过率高 持久有效
台湾超亲水防雾塑料专用 附着力好 透过率高 持久有效


